
2025-07-10
分享到
,将一款处于Ⅰ期临床实验阶段的体内CAR-T细胞疗法(CPTX2309)收入囊下。
管线之外,艾伯维还将获得Capstan专有的tLNP平台技术,旨在递送编码CAR蛋白的RNA有效载荷(mRNA或基因编辑工具),进而在体内对特定细胞类型进行重编程。
以CPTX2309为例,该疗法使用靶向CD8的tLNP,将编码CD19 CAR的mRNA靶向递送到 CD九游体育8+ T细胞,从而在体内指导CAR蛋白合成(构建CAR-T细胞),以治疗B细胞介导的自身免疫疾病,如系统性红斑狼疮、多发性硬化和类风湿关节炎。
就在今年3月,阿斯利康以10亿美元收购了另一家体内CAR-T公司EsoBiotec。在此之前,赛诺菲、安斯泰来、诺华也纷纷押注这一技术方向。
跨国药企对体内CAR-T疗法的热情持续高涨,应用前景已从血液肿瘤治疗拓展至更具挑战性的实体瘤和自身免疫疾病领域,有望引发治疗范式的根本性变革。
在这场全球性的前沿疗法竞速中,LNP递送作为关键底层技术,为体内CAR-T疗法的突破性进展提供了重要支撑。
更令人惊喜的是,人工智能、量子计算与高通量实验平台的引入,正在推动LNP设计优化从经验驱动迈向数据驱动,提高候选药物研发效率的同时,为更多复杂疾病带来全新思路。
艾伯维的收购印证,LNP递送技术正突破疫苗边界,展现出应用于细胞疗法、基因编辑等新型疗法的巨大潜力,行业处在价值重构的关键时刻。

作为免疫细胞疗法中进展最快、发展最为成熟的技术,CAR-T以其卓越的治疗潜力和优异的治疗效果而备受关注,目前FDA共批准7款CAR-T细胞疗法,2024年全球销售总额达45亿美元,预计到2030年这一数字将提升至218亿美元。
尽管CAR-T前景广阔,然而传统方法需要从患者体内提取细胞,在体外进行基因改造,再通过免疫细胞清除后回输至患者体内,整个过程耗时耗力,提高了治疗成本,极大降低了患者可及性。
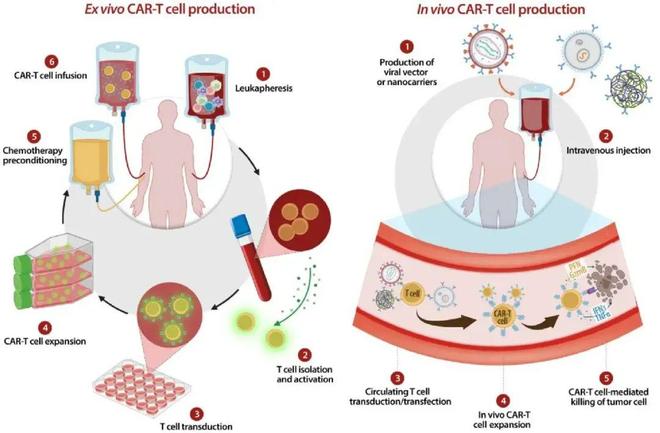
体内CAR-T则有望解决这一挑战,通过直接在患者体内改造免疫细胞,有望大幅简化治疗流程、缩短生产周期,“让成本降低一个数量级”,从而打开更大的市场空间。
而这也并非艾伯维首次押注体内CAR-T,去年1月,艾伯维与Umoja Biopharma宣布达成总价值14.4亿美元的合作,以利用Umoja专有的慢病毒载体平台开发多款CAR-T疗法。
体内CAR-T疗法的核心挑战,在于如何将CAR构建体精准、高效且安全地递送至目标T细胞,由此诞生出慢病毒载体、LNP递送等不同技术路线。
而与LNP递送相比,慢病毒载体存在靶向性不足、生产成本较高等缺点,尤其是在最关键的安全性问题上,慢病毒载体将外源DNA整合到宿主基因组,存在潜在风险。与之相比,LNP递送具有良好的安全性和生物相容性。
于是,艾伯维近期在体内CAR-T领域的一系列动作值得深入解读:先是与慢病毒载体技术领先企业达成合作,随后又以显著更高的交易金额收购LNP递送公司,这背后是其对不同技术路径的重新考量。
从先后顺序与交易细节能够感受出,艾伯维针对LNP递送的战略意图更加明显,反映出其对这一技术路径在解决体内CAR-T关键挑战方面所寄予的厚望。

mRNA,即信使核糖核酸(Messenger RNA),是一种携带遗传信息的分子,作为DNA和蛋白质之间的桥梁,指导蛋白质生产。
理论上,我们可以利用mRNA合成任何想要的蛋白质,来达到治愈疾病的效果,也难怪,马斯克会将mRNA技术称为“人类医学的未来”。
但由于其大小、电荷和可降解性,mRNA需要递送技术来确保精准靶向并发挥作用,脂质纳米粒(LNP)是目前主流的载体递送方式。
LNP的技术价值不言而喻,作为一项革命性的递送手段,其显著提高了mRNA的有效性和安全性,辉瑞/BioNTech与Moderna的两款mRNA疫苗均采用LNP递送,为控制全球大流行立下汗马功劳。
也正因如此,开创LNP药物递送工作的皮特·库里斯(Pieter Cullis)、卡塔琳·卡里科(Katalin Karikó)、德鲁·魏斯曼(Drew Weissman)于2022年获得素有“小诺贝尔奖”的盖尔德纳奖。
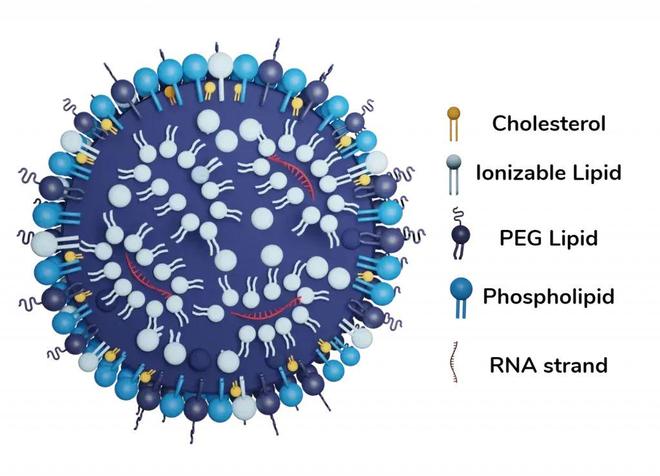
对于mRNA企业来说,找到更好的LNP递送系统成为重要的研发方向,也是衡量其技术实力和核心壁垒的关键因素。
然而,LNP递送载体的设计九游体育材料纷繁复杂、数量众多,相互间可形成数百万种不同组合,相关研究长期受限于传统方法的低效,高度依赖科研人员的经验判断,并需通过大量重复性实验进行验证,这种“大海捞针”式的研发模式不仅成本高昂,而且周期漫长。
凭借其强大的数据分析、模式识别和预测能力,AI能以惊人的速度和精准度解析组分、结构与功能间的复杂关系,甚至生成全新、特定功能的脂质分子,极大拓展了LNP的设计与优化空间。
这种从“试错”到“理性设计”的范式转变,显著加速了LNP的开发进程,为更稳定、更高效、更安全且具靶向性的下一代LNP递送系统铺平道路。
BioNTech已在所有核心业务领域全面部署了AI,在其首席执行官兼联合创始人Ugur Sahin看来,公司正处于整合先进AI技术以彻底革新个体化医疗的最前沿。
2023年,BioNTech以5.62 亿英镑战略性收购了AI公司InstaDeep,成为公司发展历程中的一个关键里程碑。
通过此次收购,BioNTech计划在其发现平台中无缝嵌入InstaDeep经过验证和创新的 AI 和机器学习模型,并利用InstaDeep的DeepChain™平台进行连接,进一步集成自动化实验室基础设施。
DeepChain™ 平台集成了多款先进的生物AI模型,包括 ProtBFN(蛋白质设计)、AbBFN(抗体设计)以及DNA基础模型(Nucleotide Transformer 和SegmentNT)。同时,这个平台大大降低了 AI 部署和应用门槛,研发人员仅需数行代码即可访问复杂的工作流程,以高效的微调方法定制模型,并与AI助手Laila通过自然语言协作。
这种人机交互模式已在BioNTech位于美因茨的实验室中得到验证:Laila通过自动化任务处理,显著提升了生产力,让科学家能专注于更有创造性的研究。
另一份官方文件显示,公司研发重点方向便是利用高通量筛选平台探索新型药物递送方式。AI与高通量平台的融合,正持续加快BioNTech在LNP开发方面的进程。
另一个案例则是赛诺菲,这家老牌疫苗企业曾被认为落后于mRNA技术的浪潮,如今公司希望借助AI的力量奋起直追。
2023年6月,赛诺菲宣布“All in”人工智能和数据科学,为患者加速取得突破性成就。
在官宣文件中,赛诺菲特别指出,AI加速了mRNA的研究工作,指出公司拥有一个庞大的LNP库,研发团队使用AI创建数字模型,将LNP预测过程的速度从数月提高到数天。
巨头们的争相应用,清晰地指向了一个结论:决胜下一代疗法的跑道上,脂质纳米颗粒(LNP)的开发、设计和优化已经扮演着不可或缺的重要角色。而能否充分发挥AI的赋能作用,将直接决定哪些选手能在这场激烈的竞赛中率先撞线。

当DeepSeek的问世证明中国AI已跻身全球顶尖水平时,另一个关键问题浮出水面:在更具挑战性的AI制药领域,尤其是在关键的LNP(脂质纳米颗粒)赛道上,中国企业能否复刻这样的突破?
据智药局观察,剂泰科技、艾博生物、云顶新耀、海昶生物、沙砾生物等企业均已深度布局LNP领域。
这些公司正基于各自的独特优势,探索并形成了差异化的开发路径,正是这种战略上的分野,正在塑造着截然不同的成长轨迹与价值实现模式。
有的致力于优化LNP组分与配方,如海昶生物构建的四价-三价脂质纳米粒(QTsome®)基因递送平台,优化了核酸药物的负载并提高了细胞内递送效率。
有的侧重开发靶向递送策略,如云顶新耀开发的tLNP系统,能够引导编码CAR的mRNA在T细胞中特异且高效地表达,已获得多项临床前验证。
作为国内纳米递送领域少有的AI-native公司,剂泰科技值得更多关注和期待,公司在技术平台、团队成员、商业进程、资金储备等多元维度具备全面竞争力,以AI创新弯道超车,值得期待。
AI驱动的制剂开发及药物递送是一个挑战巨大的前沿赛道,部分领域近乎“拓荒”,首先要面临的核心困境便是数据的严重匮乏。
与小分子药物主要关注单一分子与靶点蛋白的结合不同,药物递送涉及一个分子与多个不同分子之间的结合过程,要理解这种动态相互作用及最终形成何种构型,行业缺乏公开的高质量数据作为支撑。
在成立之初,剂泰便打造了专有的高通量+ AI制剂平台,该平台能针对不同递送途径仿真物理参数,可产生万级小分子、核酸处方/周,积累大量实验数据。
值得注意的是,与小分子药物研发和蛋白质设计领域不同,LNP递送系统缺乏可直接应用的成熟算法模型,这一技术空白要求企业必须从底层构建全新的计算模型,这是对企业核心技术能力的重大考验。
剂泰科技运用量子化学、分子动力学模拟结合机器学习/深度学习算法,从零开始,创新研发了可电离脂质生成和设计以及LNP纳米材料设计和模拟的开创性人工智能和计算模拟算法。
当大语言模型背后的灵魂——Transformer架构兴起后,剂泰将其引入到脂质开发,建立了世界首个METiS LipidLM脂质语言模型和PhatGPT脂质生成模型。
更重要的是,通过将CADD、量子力场计算工具与高通量实验平台结合,剂泰构建了AI驱动的干、湿实验迭代系统,通过计算分析的与实验验证的闭环,让公司的技术平台具备了快速反馈、持续进化的能力,展现出巨大潜力。
尤其值得关注的是剂泰科技自主研发的AiLNP平台。AiLNP是全球首个高通量自动化LNP设计平台。基于自主开发的设计脂质材料的De novo生成算法,公司构建了全球第一个基于高通量微流控LNP组装筛选平台Datalots®,以及具备自主知识产权的百万级脂质库,实现了“全域”设计空间探索,快速高效定位出最优的LNP。
然而,技术平台的先进仅仅是必要条件,能否将尖端技术成功转化为实际药物研发成果,才是对企业实际价值的真正考验。
通过整合先进的干湿迭代平台与跨学科专家团队,剂泰科技在研发领域落地一系列成果,对标国际巨头,以后来者姿态在部分领域实现了追赶超越。
据公开资料,在肝靶向领域,剂泰科技达到了best-in-class水平,递送效率大幅超越行业巨头。在肺靶向等领域, 对标海外顶尖药企也都达到数量级的药效提升。此外,公司在全身肌肉、脑、免疫器官、肿瘤的靶向递送技术上也有重大突破。
据悉,目前剂泰已与多家全球顶尖药企和生物技术公司建立深度合作,共同推动创新药物的研发与商业化进程。
当然,对于当前国内AI制药行业,尤其是在AI+LNP前沿领域探索的企业而言,摆在面前更为现实的问题是如何确保充足的资金支持,以持续保持技术领先地位并推进研发和商业化进程。
在纳米递送的细分赛道,剂泰科技的融资也颇为引人注目。自2020年1月成立至今,剂泰累计获得红杉中国、中金资本、五源资本、人保资本、峰瑞资本等头部资本近3亿美元的融资,资金储备充沛,兵强马壮。
艾伯维的重磅收购标志着基于mRNA-LNP的体内CAR-T疗法已迎来拐点,凸显出药物递送的关键价值。
展望未来,作为基因编辑、细胞疗法、RNA药物等新兴疗法的关键技术,LNP递送在打开更广阔的临床应用空间,而随着AI技术的深度赋能,这一领域还将释放出更大的创新潜能和市场价值。
尽管国内LNP递送的开发起步晚于国际同行,但通过AI技术突破、量子物理模拟和高通量实验平台等创新手段,我国企业蓄势待发,将有实力与国际领军企业同台竞技。